La salud intestinal podría influir en el riesgo de enfermedad
Por Dr. Joseph Mercola, Mercola, 31 de diciembre del 2020.
HISTORIA EN BREVE
- Una parte significativa del sistema inmunológico reside en el tracto gastrointestinal. Los investigadores de Harvard identificaron la población específica de bacterias intestinales que modifican las respuestas inmunes localizadas y sistémicas para protegerse de los invasores
- Las Bacteroides fragilis y otras bacterias de la familia Bacteroides inician una señalización que ayuda a liberar el interferón beta, que combate la invasión viral al estimular las células inmunitarias para atacar el virus y provocar la autodestrucción de las células infectadas por el virus
- La permeabilidad intestinal mediada por la zonulina es importante para la patogénesis de muchas enfermedades inflamatorias crónicas. La zonulina se produce como respuesta a las bacterias dañinas, la cual elimina las bacterias al abrir las uniones estrechas
- Aparte del crecimiento excesivo de bacterias, el gluten ayuda a liberar la zonulina, ya que esta considera al gluten como un componente dañino de un microorganismo
- Las enfermedades inflamatorias crónicas relacionadas con la mala regulación de la zonulina y el intestino permeable incluyen trastornos autoinmunes, trastornos metabólicos, enfermedades intestinales, enfermedades neuroinflamatorias y cáncer cerebral y hepático
Se está prestando más atención a la salud intestinal y esto es comprensible, si consideramos que una gran proporción del sistema inmunológico reside en el tracto gastrointestinal. Como tal, es importante mejorar la salud del microbioma intestinal, ya que tendrá muchos efectos en la salud física y emocional.
La evidencia científica también sugiere que la nutrición se enfoca en nutrir las bacterias que promueven la salud en el intestino (y en otras partes del cuerpo). Al hacerlo, aleja a los microbios dañinos y refuerza la protección frente a las enfermedades crónicas.
La enfermedad comienza en el intestino
Algunos de los problemas de salud influenciados por el microbioma intestinal incluyen: TDAH, autismo, problemas de aprendizaje, obesidad, diabetes y enfermedad de Parkinson. Una revisión científica del año 2020 concluyo que toda enfermedad inflamatoria comienza en el intestino. La higiene excesiva es una de las causas principales. Es decir, la limpieza excesiva puede ser perjudicial.
Pero la alimentación también es importante. El artículo aborda la función de la permeabilidad intestinal mediada por la zonulina en la patogenia de las enfermedades inflamatorias crónicas (EIC). De acuerdo con el autor, el Dr. Alessio Fasano, un gastroenterólogo pediatra, investigador y director del Centro de Investigación y Tratamiento de la Celiaquía:
“Los tres elementos que causan EIC son la composición genética, exponerse a desencadenantes ambientales, una mayor permeabilidad intestinal (que puede agravarse por la composición de la microbiota intestinal), la agresividad del sistema inmunológico responsable del equilibrio de la tolerancia y la respuesta inmune, así como la composición del microbioma intestinal y su influencia en la expresión genómica.
Durante la última década, muchas publicaciones se han enfocado en la genética humana, el microbioma intestinal y la proteómica, lo que sugiere que la pérdida de la barrera mucosa, en especial en el tracto gastrointestinal, puede afectar el tráfico de antígenos, lo que influye en la interacción bidireccional entre el microbioma intestinal y el sistema inmunológico.
Esta interferencia influye mucho en la configuración del sistema inmunológico del intestino, así como en el cambio de la predisposición genética al resultado clínico. Esta observación genero una revisión de las posibles causas de las epidemias de EIC, lo que sugiere que la permeabilidad intestinal es un factor importante.
Los estudios preclínicos y clínicos demostraron que la familia de las zonulinas, que es un grupo de proteínas que modifican la permeabilidad intestinal, está relacionada con una variedad de EIC, incluyendo las enfermedades autoinmunes, infecciosas, metabólicas y tumorales. Estos datos ofrecen nuevos objetivos terapéuticos para una variedad de EIC en los que la vía de la zonulina está relacionada con su patogenia”.
Las bacterias gobiernan la salud
El Dr. Fasano señala que no tenemos suficientes genes para explicar la infinidad de enfermedades crónicas que pueden dañarnos. Los genes tampoco pueden explicar cuándo puede aparecer una enfermedad. Para resolver estos misterios, debemos observar al microbioma, ya que “la interacción entre nosotros y el entorno dicta nuestro destino clínico”.
La condición de la mucosa intestinal también es importante, además de los microbios. “Aunque esta interfaz mucosa (200 m2) no es visible, es un factor importante a través de sus interacciones con una variedad de factores que provienen de nuestro entorno, incluyendo microorganismos, nutrientes, contaminantes y otros materiales”, explica Fasano.
Aunque las uniones intracelulares solían considerarse estáticas e impermeables, ahora sabemos que no es el caso. Como explica Fasano, la zonulina modula la permeabilidad intestinal. Sin embargo, aunque la zonulina es un biomarcador de la permeabilidad intestinal y es un factor importante en muchas enfermedades inflamatorias crónicas, el intestino permeable no causa todas las EIC.
Eventos que desarrollan las EIC
El gráfico a continuación, incluido en la revisión de Fasano pero que procede de un artículo anterior titulado como “Zonulin, a Regulator of Epithelial and Endothelial Barrier Functions, and Its Involvement in Chronic Inflammatory Diseases”, coescrito por Fasano y Craig Sturgeon, detalla los “eventos que desarrollan las enfermedades inflamatorias crónicas”.
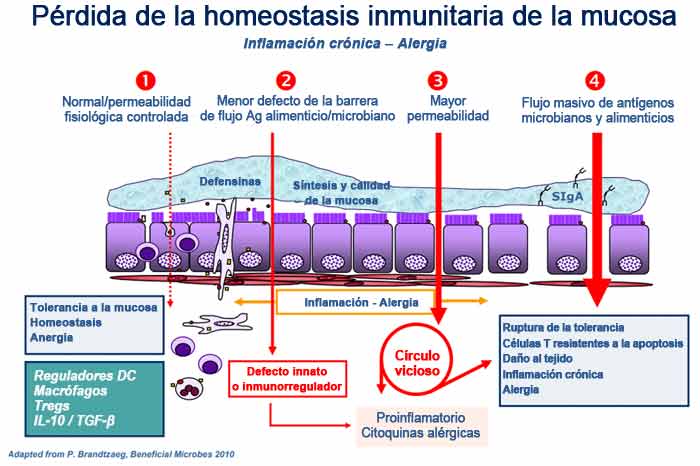
En circunstancias normales, se mantiene una homeostasis saludable en el revestimiento del intestino, de modo que cuando ingresa un antígeno, no se produce una reacción excesiva (anergia). En el n. ° 2 del gráfico, se establece la disbiosis intestinal (es decir, un desequilibrio en la cantidad y diversidad de la microbioma intestinal), lo que provoca una mayor producción de zonulina, que a su vez aumenta la permeabilidad del revestimiento intestinal.
De acuerdo con Fasano, el crecimiento excesivo de bacterias y el gluten son los dos desencadenantes más poderosos de la liberación de zonulina. La zonulina se produce como respuesta a las bacterias dañinas. Ayuda a eliminar las bacterias al abrir las uniones estrechas, por lo que es lógico el crecimiento excesivo de bacterias. Pero, ¿por qué responde al gluten?
Resulta curioso que la zonulina considera al gluten como un componente dañino de un microorganismo. Por esta razón el gluten causa la liberación de zonulina. Aunque Fasano no lo menciona, el herbicida glifosato también activa la zonulina y es mucho más potente que el gluten.
La permeabilidad posterior permite que el antígeno derivado de la microbiota y la endotoxina migre desde el flujo luminoso a la lámina propia (el tejido conectivo que forma parte de la membrana mucosa que recubre el intestino), lo que genera la inflamación.
A medida que el proceso continúa empeorando (número 3 en el gráfico), se activa la respuesta adaptativa, lo que genera la producción de citoquinas proinflamatorias, incluyendo el interferón gamma (IFN-γ) y el factor de necrosis tumoral alfa (TNF-α). Estas citoquinas empeoran aún más la permeabilidad, lo que crea un círculo vicioso. Al final (No. 4), se descompone la tolerancia de la mucosa por completo, lo que resulta en una enfermedad inflamatoria crónica.
Enfermedades inflamatorias crónicas relacionadas con el intestino permeable
La enfermedad inflamatoria crónica que surge de todo esto depende de la composición genética, en parte por los tipos de exposición y por la composición del microbioma intestinal. Como explica Fasano:
“Además de la predisposición genética y la exposición a factores ambientales, la patogenia de muchas EIC parece involucrar cambios por la permeabilidad intestinal/tráfico de Ag, la activación inmune y cambios en la composición/función del microbioma intestinal.
La zonulina modula las funciones de la barrera epitelial y endotelial. La disbiosis intestinal puede liberar zonulina que genera la transferencia del contenido luminal a través de la barrera epitelial, lo que provoca la liberación de citoquinas proinflamatorias que provoca una mayor permeabilidad y establece un círculo vicioso que genera una afluencia masiva de Ag alimenticios y microbianos que activan las células T.
Dependiendo de la composición genética, las células T pueden permanecer dentro del tracto gastrointestinal, lo que causa EIC del intestino, o pueden migrar a varios órganos diferentes para causar EIC sistémica”.
Las enfermedades inflamatorias crónicas relacionadas con la mala regulación de la zonulina incluyen:
- Trastornos autoinmunes como enfermedad celíaca, diabetes tipo 1, enfermedad inflamatoria intestinal, esclerosis múltiple y espondilitis anquilosante
- Desordenes metabólicos tales como obesidad, resistencia a la insulina, enfermedad del hígado graso no alcohólico, diabetes gestacional, hiperlipidemia y diabetes tipo 2
- Enfermedades intestinales como el síndrome del intestino irritable, la sensibilidad al gluten no celíaca y la disfunción entérica ambiental (una enfermedad crónica que afecta al intestino proximal)
- Enfermedades neuroinflamatorias como el trastorno del espectro autista, esquizofrenia, trastorno depresivo y fatiga crónica/encefalomielitis miálgica
- Cáncer cerebral y hepático
Los microbios intestinales influyen en los genes y en el riesgo de cáncer
Aunque la inclusión del cáncer puede parecer extraña, algunos investigadores consideran que el microbioma intestinal puede ayudar a prevenir y tratar el cáncer.
No solo se ha demostrado que las bacterias intestinales influyen en la expresión genética, al activar algunos genes y desactivar otros, la investigación publicada en el año 2018 encontró que los microbios intestinales controlan las respuestas inmunitarias antitumorales en el hígado y que los antibióticos pueden alterar la composición de las células inmunes en el hígado, lo que causa el crecimiento tumoral.
Los investigadores de la Facultad de Medicina de Harvard han identificado la población de microbios intestinales que modifican la respuesta inmune localizada y sistémica para protegerse de los invasores.
Ciertas bacterias intestinales también promueven la inflamación, que es un factor subyacente en casi todos los tipos de cáncer, mientras que otras bacterias la detienen. Incluso se ha demostrado que la presencia de ciertas bacterias intestinales estimula la respuesta a los medicamentos para combatir el cáncer.
Una forma en que las bacterias mejoran la eficacia del tratamiento contra el cáncer es al activar el sistema inmunológico y permitir que funcione de mejor manera. Los investigadores descubrieron que es posible que ciertos medicamentos no funcionen en absoluto cuando estos microbios están ausentes.
Las bacterias intestinales son parte de la defensa antiviral
La investigación demuestra que las bacterias intestinales están involucradas en la defensa antiviral. De acuerdo con lo reportado por la Facultad de Medicina de Harvard el 18 de noviembre de 2020:
“Por primera vez, los investigadores de la Facultad de Medicina de Harvard identificaron la población específica de microbios intestinales que modifica la respuesta inmunitaria localizada y sistémica para protegerse de los invasores. La investigación identifica un grupo de microbios intestinales y una especie que hace que las células inmunes liberen interferones tipo 1, que son químicos que repelen los virus.
Los investigadores identificaron la molécula compartida por muchas bacterias intestinales que desbloquea la protección inmunológica. Según los investigadores, dicha molécula no es difícil de aislar y podría convertirse en la base de los medicamentos que refuerzan la inmunidad antiviral”.
Aunque aún se deben confirmar y replicar los ensayos, apuntan a la posibilidad de que pueda mejorar la inmunidad antiviral al repoblar el intestino con Bacteroides fragilis y otras bacterias de la familia Bacteroides.
Estas bacterias inician una señalización que genera la liberación de interferón beta para combatir la invasión viral al estimular a las células inmunitarias para que ataquen al virus y provoquen la autodestrucción de las células infectadas.
“Sobre todo, una molécula que reside en la superficie de la bacteria ayuda a liberar el interferón beta al activar la señalización conocida como TLR4-TRIF”. Harvard explica. “Esta molécula bacteriana estimula la señalización inmunológica que se activa por uno de los nueve receptores tipo toll (TLR) que forman parte del sistema inmunológico innato”.
Importancia de la vitamina D
La investigación también destaca la importancia de la vitamina D en la salud intestinal y en la autoinmunidad sistémica. El artículo, publicado el 21 de enero de 2020 en Frontiers in Immunology, señala lo siguiente:
“Las enfermedades autoinmunes tienden a compartir una predisposición a la deficiencia de vitamina D, que altera el microbioma y la integridad de la barrera epitelial intestinal.
En esta revisión, resumimos la influencia de las bacterias intestinales en el sistema inmunológico, exploramos los patrones microbianos que han surgido sobre las enfermedades autoinmunes y explicamos cómo la deficiencia de vitamina D puede contribuir a la autoinmunidad a través de los efectos sobre la barrera intestinal, la composición del microbioma o los efectos directos sobre las respuestas inmunitarias”.
Como se señaló en esta revisión, la vitamina D tiene varios efectos directos e indirectos en el sistema inmunológico, incluyendo promover las células T reguladoras (Tregs), inhibir la diferenciación de las células Th1 y Th17, deteriorar el desarrollo y la función de las células B, reducir la activación de los monocitos y estimular los péptidos antimicrobianos de las células inmunes.
Dicho esto, la relación entre la vitamina D y la autoinmunidad es complicada. Aparte de la inmunosupresión, la vitamina D parece mejorar los trastornos autoinmunes por la forma en que afecta la composición de la microbiota y de la barrera intestinal.
La revisión cita investigaciones que demuestran que los niveles de vitamina D alteran la composición del microbioma intestinal. En general, la deficiencia de vitamina D tiende a aumentar la población de Bacteriodetes y Proteobacteria, mientras que un mayor consumo de vitamina D tiende a aumentar la prevalencia de Prevotella y reducir ciertos tipos de Proteobacteria y Firmicutes.
Aunque la investigación aún es escasa en lo que respecta al impacto de la vitamina D en las bacterias intestinales, en especial en personas con enfermedades autoinmunes, la deficiencia de vitamina D y las enfermedades autoinmunes son padecimientos conocidos y a menudo se recomienda la suplementación con vitamina D para estas personas.
Vitamina D es necesaria para mantener las uniones
La vitamina D es bien conocida por apoyar las defensas de las células inmunitarias e intestinales en el intestino. De hecho, la vitamina D es uno de los componentes necesarios para mantener las uniones estrechas. Como explica esta revisión:
“El epitelio intestinal interactúa de manera constante con el entorno externo. La integridad de la barrera y la función antimicrobiana en las superficies epiteliales son importantes para mantener la homeostasis y prevenir la invasión de especies microbianas.
Un epitelio intestinal y una capa mucosa sanas son importantes para protegerse frente la invasión de organismos patógenos, mientras que la vitamina D ayuda a mantener dicha función. Muchos estudios encontraron que la señalización de vitamina D3/VDR modifica la cantidad y distribución de las proteínas de unión.
Como proteína que permite la transferencia de iones hacia el flujo luminoso, la expresión de claudina-2 en la deficiencia de vitamina D puede contribuir al desarrollo de colitis.
La vitamina D regula ascendentemente el ARNm del péptido antimicrobiano y la expresión de proteínas, incluyendo la catelicidina, defensinas y la lisozima. Los péptidos antimicrobianos, secretados por las células de Paneth en el intestino, son mediadores de la composición del microbioma. Las defensinas son secretadas por las células epiteliales, las células de Paneth y las células inmunes. Y son componentes importantes de la respuesta innata en el intestino”.
La vitamina D podría contribuir a las enfermedades autoinmunes
De acuerdo con los autores, la deficiencia de vitamina D puede contribuir a la enfermedad autoinmune al afectar el microbioma y el sistema inmunológico de la siguiente manera:
- La deficiencia o la suplementación de vitamina D modifica el microbioma, mientras que manipular la composición bacteriana afecta la manifestación de la enfermedad.
- La falta de señalización de vitamina D debido a una deficiencia puede afectar la integridad de la barrera física y funcional del intestino, lo que permite que las interacciones bacterianas estimulen o inhiban las respuestas inmunitarias.
- Las defensas inmunológicas pueden verse comprometidas si sufre de una deficiencia de vitamina D.
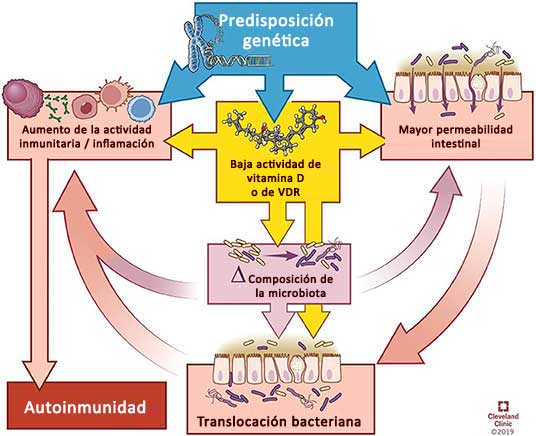
Cómo mejorar el microbioma intestinal
Toda esta información debería enfatizar la importancia de mejorar el microbioma intestinal y el nivel de vitamina D para una buena salud. Al repoblar el intestino con bacterias beneficiosas, es posible controlar los microbios y hongos patógenos al evitar que se reproduzcan, mientras que mejorar los niveles de vitamina D ayudará a evitar el intestino permeable.
Consumir alimentos fermentados es la maneras más fácil, efectiva y económica de mejorar la salud del microbioma intestinal. Las opciones saludables incluyen lassi (un Bebida de yogur indio), productos lácteos orgánicos de vacas alimentadas con pastura, como kéfir, yogur, natto (soya fermentada) y vegetales fermentados de todo tipo.
Aunque no recomiendo tomar muchos suplementos (ya que creo que la mayoría de los nutrientes deben provenir de los alimentos), los probióticos son una excepción si no consume alimentos fermentados de manera regular. Los probióticos a base de esporaspueden ser muy buenos cuando está tomando antibióticos. También ayudan a complementar los probióticos habituales.
Los probióticos a base de esporas, que consisten de la pared celular de las esporas de bacilo, ayudan a fomentar la tolerancia inmunológica y no se ven afectados por los antibióticos debido a que solo contienen las esporas de bacilo, que es la capa que protege el ADN y su mecanismo de trabajo.
Tal vez ya sepa que los antibióticos matan las bacterias intestinales, tanto las buenas como las malas. Por esta razón las infecciones secundarias y una mala función inmunológica son efectos secundarios de los antibióticos. Tomar bajas dosis de antibióticos de manera constante a través de los alimentos también afecta el microbioma intestinal, lo que puede provocar una enfermedad crónica y un mayor riesgo de resistencia a los medicamentos. Por último, pero no menos importante, también es bueno evitar los factores que dañan el microbioma, los cuales incluyen:
- Consumir antibióticos, a menos que sean muy necesarios
- Consumir carne criada de manera convencional y otros productos animales, ya que estos animales consumen muchos antibióticos, además de granos GM o tratados con glifosato
- Consumir alimentos procesados (ya que el exceso de azúcares alimenta a las bacterias patógenas)
- Consumir agua clorada y fluorada
- Utilizar jabón antibacterial y productos que contienen triclosán